慢性压力管理(专业版)
现代生活中压力无处不在,每个人都时刻感觉到压力。有的压力对人体生理健康是必须的,但大部分压力尤其慢性压力却是有害的,导致如消化系统问题、头痛、失眠、情绪和心理症状等
其他名称:慢性应激;心理应激
英文名称:Chronic Stress Management,Chronic Stress,Psychological Stress
应激反应分为急性和慢性2种:
研究表明,慢性应激是导致压力性/应激性心肌病(Stressful/Takotsubo Cardiomyopathy)或心碎症候群(Broken Heart Syndrome)的最主要因素之一。应激性心肌病是一种自发性的心脏衰弱,使患者容易发生心律失常,甚至心脏性猝死。虽然机制尚不清楚,但一般认为慢性应激引起的肾上腺素过度升高刺激心肌,以及改变其功能并引起心房重塑等有关。
人。点击了解更多相关内容: 心碎症候群 >>
1.身体对压力的反应
当个体经历身体或精神、内源或环境等压力源时,机体将启动复杂的适应性压力系统。这种反应过程导致肾上腺应激激素(即糖皮质激素)和儿茶酚胺的释放,以刺激身体有关系统的适应性变化。
2.“战斗或逃跑”应激反应
3.了解皮质醇作用:皮质醇是肾上腺分泌的最主要应激激素。适量的皮质醇是维持最佳健康所必需的,但过多或过少都可造成损害。其主要功能是:
4.认知机体对压力反应过程
研究表明,每个人天生适应压力能力是不同的。然而,耐受性是可变的,因为一些人只能处理低水平和短持续时间的压力,而另一些人则可以在更长时间内适应更高水平的压力。1935年,美国H. Selye博士提出了压力/应激概念,并指出在处理压力时身体会面临三种状态:
附注:关于“肾上腺疲劳(Adrenal Fatigue)问题:
“肾上腺疲劳”是涉及压力问题的替代医学常用术语,虽然还没有得到传统医学的公认诊断。“肾上腺疲劳”的症状是由多因素病理过程引起的,其中包括HPA轴。
此外,艾迪生病或称为“肾上腺皮质功能不全”,是一种可能危及生命的疾病。它主要是自体免疫性疾病的结果,但也可能由遗传异常引起。艾迪生病比压力引起的后果更为严重,应由合格的医疗专业人员密切监测、诊断和治疗。
与慢性压力有关的症状常见如下:
调整饮食与生活方式
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于慢性应激管理的营养和草本补充剂,主要包括如下:
1. 维生素C:
肾上腺具有体内最高浓度的维生素C1。除了其众所周知的自由基清除剂功能外,维生素C还是儿茶酚胺合成的辅助因子,儿茶酚胺是参与应激反应的神经激素,有助于调节中枢神经系统的活动1-3。在应激或感染期间,血液和白细胞中的维生素C水平会迅速下降4,而抑郁和焦虑症状与维生素C的低摄入和低循环水平有关2。
在一项对照临床试验中,压力诱导的焦虑和抑郁患者的维生素C以及维生素E和A水平低于健康受试者,与单独的抗抑郁治疗相比,在抗抑郁治疗中添加这些营养素维生素C、维生素E和β-胡萝卜素(维生素A)可以更大程度地减轻焦虑和抑郁症状5。另一项对照试验发现,在健康的高中生中,每天补充500mg维生素C可以减少焦虑水平,降低平均心率6。此外,一项研究综述表明,高剂量的维生素C可以减轻焦虑,缓解与压力相关的血压升高7。
2. 维生素B族与复合维矿素:
B族维生素缺乏与神经精神疾病有关,如抑郁症、阿尔茨海默病、精神分裂症和其他类型的精神病和痴呆症,健康的神经系统功能需要充足的所有B族维生素8,9。
多种维生素减轻压力和疲劳的能力已经在许多试验中得到证实10-12。在一项针对60名工作成年人的随机对照试验中,那些连续12周每天服用高剂量复合B族维生素的人与服用安慰剂的人相比,压力、困惑和抑郁情绪水平较低13。一项研究综述得出结论,复合维生素,特别是复合维生素B补充剂,可以有效地降低感知压力,减轻轻度精神症状,改善健康个体的日常情绪14。
B族维生素也可以支持正常的HPA轴功能。在一项有138名受试者参与的安慰剂对照试验中,补充含有B族维生素的复合维矿素16周后,皮质醇唤醒反应增强。皮质醇觉醒反应发生在醒来后约30分钟,通常导致一天中最高的皮质醇水平,被认为是健康的下丘脑轴张力的标志,并且与一天中其余时间较低的痛苦水平有关15。另一项随机对照交叉试验检测了240名承受剧烈身体压力的中国军人服用一周复合维生素补充剂的效果。复合维生素与正常下丘脑轴功能的更好恢复和心理症状的改善有关16。
3. 欧米伽3脂肪酸:
ω-3脂肪酸(EPA和DHA)可能有助于预防和治疗压力、焦虑和抑郁17-19。血液中EPA和DHA的低水平与压力的几个生物学指标有关:炎症标志物升高、神经系统信号传导失调和HPA轴高活性20,21。相反,ω-6脂肪酸主要通过食用动物脂肪和加工植物油获得,可促进炎症,从而诱导应激信号,并导致应激相关疾病18。
在一项针对甘油三酯水平高的参与者的随机对照试验中,连续八周服用3400mg EPA和DHA会增加心率变异性,表明与压力相关的神经系统信号较低;然而,每天850mg的较低剂量没有效果22。另一项对照试验发现,在住院治疗计划中,每天60mg EPA和252mg DHA的三周治疗改善了酒精受试者的压力和焦虑,并降低了皮质醇水平23。抑郁症患者的试验证据表明,ω-3脂肪酸可以纠正HPA过动,减轻症状,并可能提高对抗抑郁治疗的反应性21,24。
4.丝氨酸磷脂:
磷脂酰丝氨酸存在于细胞膜中,有助于促进健康的细胞通讯。它调节组织对炎症的反应,并可以减少氧化应激25。多项研究表明,丝氨酸磷脂可以平衡HPA轴信号传导,并可能限制肾上腺过度激活的负面后果。
在一项针对75名健康男性志愿者的试验中,在报告慢性压力水平高的男性亚群中,服用每组提供400mg磷脂酰丝氨酸及其前体磷脂酸的补充剂42天,降低了HPA轴对急性压力的反应26。在其他临床研究中,同样的组合被注意到可以减轻对精神压力的应激反应27。而每天单独服用300mg磷脂酰丝氨酸可以减少感知到的压力,改善容易产生焦虑、担心和恐惧等健康年轻人的情绪28。磷脂酰丝氨酸也被发现可以降低皮质醇水平,降低男性急性运动时的皮质醇反应,这种效果可能有助于防止过度训练的有害后果,如表现下降、受伤、免疫抑制和心理健康的恶化29。
5. 色氨酸:
L-色氨酸是神经递质血清素的一种氨基酸前体。血清素与应激反应有着复杂的关系30。应激性炎症似乎会导致色氨酸的过度分解,这可能会减少血清素的产生,增加抑郁的风险31;此外,色氨酸耗竭已被证明可增加应激敏感性32。
对健康成人的研究表明,每天补充800到2800mg的色氨酸,可降低皮质醇对压力的反应,减轻与压力相关的负面情绪,并防止一些人的压力性进食33-35。在一项随机对照试验中,富含色氨酸的水解蛋白补充剂在急性应激反应中增加积极情绪并降低皮质醇释放36。
6.益生菌和益生元:
肠道微生物组、神经系统和HPA轴紧密相关。益生菌和益生元可以改善肠道细菌的平衡,越来越多的证据表明,它们有可能对压力反应产生积极影响17,36,38。研究表明,益生菌可以降低压力反应性和焦虑,改善情绪、记忆力和认知,导致一些研究人员将具有这些作用的益生菌称为“心理益生菌(Psychobiotics)”39。
在几项试验中发现,用干酪乳杆菌菌株Shirota(代田菌)制成的发酵乳制品可以抑制皮质醇在压力下的升高,并减少健康医学生的压力相关健康问题,如抑郁或焦虑情绪、消化不良和感冒症状40-42。在一项随机对照试验中,每天补充100亿CFU 植物乳杆菌299v、连续10天,可降低即将进行检查的学生的唾液皮质醇水平43。在其他对照试验中,以每天30亿CFU的剂量服用瑞士乳杆菌R0052和长双歧杆菌R0175(Lallemand益生菌专有品牌CEREBIOME®)的组合,在30天的时间里,健康志愿者的感知压力和尿皮质醇水平的评分降低了44,并且在四周内每天补充10亿CFU的长双歧杆菌菌株1714抑制了皮质醇的升高和与急性压力相关的主观焦虑45。
益生元在临床研究中也显示出积极作用:在一项针对45名健康成年人的试验中,连续三周服用5.5g含有低聚半乳糖的益生元补充剂,可降低清晨皮质醇水平,并更平衡地处理积极和消极的情绪刺激46。
7.茶氨酸:
L-茶氨酸具有抗应激作用。大量研究发现,茶和茶氨酸可以降低感知到的压力和压力反应的生理标志物,包括血压、心率、皮质醇水平和大脑活动模式47。在一项包括20名药学学生的试验中,一周内每天两次服用200mg茶氨酸,比安慰剂更能降低早晨唾液α-淀粉酶水平。此外,服用L-茶氨酸的受试者报告的主观压力明显低于安慰剂组48。
L -茶氨酸的短期效果在另一项随机对照试验中得到证实,该试验有36名年龄在18至40岁之间的健康参与者参加:单次200mg剂量的茶氨酸在给药后一小时降低了主观压力,在给药后三小时降低了对认知压力源的皮质醇反应。此外,在焦虑倾向测试中得分较高的一部分参与者中,茶氨酸增加了与放松相关的脑电波活动49。
日本研究人员进行的一系列小型试验发现,在实验室进行的应激算术测试中,补充L-茶氨酸可以防止心率升高。服用L-茶氨酸的人,在应对应激任务时,唾液免疫球蛋白A(s-IgA)水平也会降低。研究人员得出结论,服用L-茶氨酸的受试者心率和s-IgA的降低可能归因于交感神经系统活动的减弱50。
茶氨酸还被证明可以对抗咖啡因的压力诱导作用,增强集中注意力51。一项为期两个月的临床试验指出,茶氨酸与维生素/矿物质/草药补充剂相结合,可以降低老年人的感知压力评分,改善认知功能52。
8. γ-氨基丁酸:可改善α脑电波、激活副交感神经,具有醒脑和安神促进睡眠等作用,可增强日常有关的抗压能力53,54,并改善认知功能。
注意:普通γ氨基丁酸是合成的,效果不如预期,而且作用一直存在争议。通过发酵产生的成分—γ氨基丁酸PharmaGABA®,被证实效果好且安全。
9.褪黑素:
褪黑激素与睡眠周期的关系众所周知。褪黑素在包括HPA轴在内的身体系统的昼夜节律调节中发挥着核心作用55。压力会降低褪黑激素水平并破坏身体的生物节律56。大脑内部时钟的慢性破坏,如轮班工作或失眠,会损害身心健康57,58。
补充褪黑激素可以改善睡眠量和质量,有助于恢复正常的昼夜节律59,60,这可能会减轻压力,防止与压力相关的健康恶化61。在一项研究中,在一组老年女性志愿者中,在晚上服用2mg褪黑素六个月,可以改善睡眠,提高循环的DHEA-S水平62。
10.脱氢表雄酮:
脱氢表雄酮(DHEA)是一种肾上腺激素,与皮质醇一样,它是在急性压力时分泌的,但慢性压力与低水平有关63。压力对DHEA的影响可能是将压力与健康不佳和衰老加速联系起来的因素之一64。低DHEA-S水平与骨质疏松、认知能力下降和痴呆等疾病有关,以及心血管疾病、情绪障碍和性功能障碍65。临床前和临床研究结果表明,DHEA替代疗法可能在保护衰老的骨骼和血管系统方面发挥作用,并可能有助于治疗抑郁症和性障碍65,66。
在一项随机、安慰剂对照、交叉试验中,年龄在40岁至70岁之间的13名男性和17名女性接受了为期6个月的每日50mg DHEA治疗,身体和心理健康状况显著改善67。在另一项研究中,24名健康的年轻男性服用了高剂量DHEA(每天两次,每次150mg),为期7天。受试者报告情绪有所改善,DHEA治疗导致夜间皮质醇水平降低68。
DHEA的补充剂量通常为女性每天10-25 mg,男性每天25-75 mg,但应基于DHEA-S血液水平检测。了解更多相关内容,可参阅本网站相关专文:DHEA与抗衰老 >>
11.镁:
镁是一种重要的矿物质,在数百个生物化学过程中起辅助因子的作用,包括那些参与应激反应的过程。镁可以抑制谷氨酸受体,减弱兴奋性传递,促进GABA和血清素活性69。临床前和临床研究观察到,镁水平受到应激刺激的负面影响,补充镁可以减轻压力70,71。镁水平低会进一步加剧压力,因为镁间接减少皮质醇分泌69。
研究表明,苏糖酸镁比普通镁制剂可更有效地提高脑内镁水平。此外,乙酰牛磺酸镁是一种镁的有机盐,与其他形式的镁相比,它在大脑中的生物利用度有所提高72。
12.姜黄素:
作为一种多酚,姜黄素具有很强的自由基猝灭和抗炎作用。阿育吠陀医学使用其治疗一系列炎症性疾病,包括肌肉骨骼问题、神经系统疾病、心脏病73。许多临床研究表明,姜黄素有可能减少慢性和重复压力对认知功能和情绪的影响74-77。此外,临床前证据表明,姜黄素的抗应激作用可能与其减少神经炎症和保持神经可塑性的能力有关78-80。
多项随机对照试验和三项荟萃分析表明,姜黄素可以减轻抑郁症患者的抑郁和焦虑症状81-83。一项针对60名患有职业压力相关焦虑症的参与者的临床试验,将高吸收姜黄素加胡芦巴的组合(每天1000mg)与相同剂量的标准姜黄素或安慰剂进行了比较。30天后,与服用普通姜黄素或安慰剂的参与者相比,服用姜黄素/胡芦巴组合的参与者报告压力、焦虑和疲劳减轻得更多,生活质量也得到了更大的改善84。在另一项针对80名糖尿病神经病变参与者的安慰剂对照试验中,与安慰剂相比,每天服用80mg不同的高吸收形式的姜黄素、持续8周可降低抑郁和焦虑症状评分85。在重度抑郁障碍患者中,与服用安慰剂的患者相比,每天摄入1500mg姜黄素12周的患者抑郁症状改善更大。此外,在试验结束四周后,这种益处仍然是可以测量的86。在耐力训练期间,补充姜黄素也被发现比安慰剂更好地降低运动员的感知压力水平87。
13. 厚朴和黄柏:
厚朴的活性成分厚朴酚等在临床前和临床试验中被发现具有多种有益作用,包括减轻应激88。在暴露于慢性应激的啮齿类动物中,厚朴酚等组合被发现可以使血清素和HPA轴活性正常化,增加大脑生长因子(脑源性神经营养因子,BDNF)的水平,减少神经炎症和大脑氧化应激,并预防抑郁行为89-92。
厚朴和黄柏的组合也被研究用于抗应激作用。在一项对照临床试验中,56名中等压力水平的健康受试者接受了提供250mg厚朴和黄柏补充剂或安慰剂,每天两次,持续四周。参与者接受了三次(上午、中午和晚上)唾液皮质醇测试,并在试验开始和结束时回答了情绪问卷。与安慰剂组相比,接受补充剂组的皮质醇总暴露量较低,情绪评分较好93。
研究了相同的组合补充剂对应激诱导的食欲和体重增加的影响。在一项对照试验中,与安慰剂相比,厚朴加黄柏剂量为250 mg,每天三次、持续六周,减轻了超重但健康的绝经前女性的体重增加,这些女性报告称饮食压力大,焦虑水平高于平均水平94。在另一项类似设计的试验中,厚朴和黄柏减轻了暂时的焦虑,但对长期抑郁或焦虑、食欲、睡眠或唾液皮质醇和淀粉酶水平没有影响95。
14.适应原药草:
适应原药草(Adaptogenic herbs)具有多方面的有益作用,支持身体对压力条件的内在弹性。它们通过以支持体内平衡的方式调节生物网络来发挥作用。例如,适应原可以提高能量水平,但也支持健全的睡眠。使用适应原的一些典型益处包括缓解疲劳、改善认知功能和情绪以及支持免疫系统等96-98。
15.假马齿苋:在阿育吠陀医学中历来被用于支持健康的认知功能143。许多动物研究已经证明了它的适应性潜力,指出它能够使应激激素水平和神经递质平衡正常化144,减少氧化应激145,防止神经退行性变146,并预防或逆转应激的其他负面生理和行为后果147-149。此外,在慢性应激的啮齿动物模型中,已经发现假马齿苋和一种活性成分(假马齿苋皂苷I)可以减少抑郁行为,使HPA轴功能正常化,减少脑氧化应激,并防止BDNF的下降和大脑环境中的其他变化150-152。在另一个实验室动物模型中,巴科帕也被发现可以提高应激能力和寿命153。
在一项针对17名健康成年人的初步试验中,假马齿苋标准化提取物,单剂量320mg和640mg,在一到两小时后的多任务心理测试中改善了认知表现,同时也降低了皮质醇水平,这表明其认知益处的一部分可能与减压效果有关154。在一项对54名老年受试者的随机对照试验中,与安慰剂相比,每天300mg的假马齿苋持续12周可改善认知能力,降低抑郁和焦虑评分,并降低心率155。
16.藏红花:藏红花是一种药食同源的药草,具有镇静、适应和其他特性。几项临床试验表明,藏红花有助于治疗轻度至中度抑郁症156,157。藏红花及其活性成分番红花素在动物研究中也显示出抗应激和抗焦虑的作用,临床前证据表明,它可能部分通过调节HPA轴反应来发挥其益处158-161。此外,另一种来自藏红花的活性化合物被发现可以预防大鼠应激诱导的抑郁行为162。
在一项随机对照试验中,没有抑郁症但报告情绪低落的受试者接受了为期四周的每天28mg藏红花提取物的治疗,与接受安慰剂治疗的人相比,他们的情绪得到了更大的改善,压力和焦虑症状也得到了减轻163。
17. 香蜂草:植物薄荷科家族成员之一,既是食用香料,作为草药可放松和振奋神经系统164,165。在食物或饮料中食用发现,香蜂草通常能改善健康年轻成年人的情绪和认知表现166。在暴露于实验压力的健康受试者中,个别剂量的香蜂草具有急性抗应激和增强认知的作用,并提高了自我报告的平静和警觉167。
在一项针对20名轻度至中度焦虑和失眠的压力志愿者的试点试验中,19名(95%)参与者每天两次用300mg香蜂草提取物治疗15天,症状得到改善。此外,14名参与者的焦虑完全缓解,17人失眠缓解,14人焦虑和失眠都得到缓解168。在一项针对80名稳定型心绞痛患者的安慰剂对照临床试验中,每天3g香蜂草提取物持续8周,可以减轻焦虑、抑郁和压力,改善睡眠169。在动物研究中,香蜂草减轻了应激引起的肠易激综合征症状170。
更多内容可点击其个性化的综合干预方案如下:
以及参阅本网如下专文的相关内容:
医疗干预
常规治疗:主要使用精神类药物治疗压力失衡引起的症状。但无法解决与压力有关的生化异常,如肾上腺激素紊乱等。
然而,采取下列措施有助于减少压力的发生或其负面作用:
参考文献:
1. Figueroa-Méndez R et al. Vitamin C in Health and Disease: Its Role in the Metabolism of Cells and Redox State in the Brain. Front Physiol. 2015;6:397.
2. Kocot J et al. Does Vitamin C Influence Neurodegenerative Diseases and Psychiatric Disorders? Nutrients. Jun 27 2017;9(7).
3. Han QQ et al. Preventive and Therapeutic Potential of Vitamin C in Mental Disorders. Curr Med Sci. Feb 2018;38(1):1-10.
4. Chambial S et al. Vitamin C in disease prevention and cure: an overview. Indian J Clin Biochem. Oct 2013;28(4):314-328.
5. Gautam M et al. Role of antioxidants in generalised anxiety disorder and depression. Indian J Psychiatry. Jul 2012;54(3):244-247.
6. De Oliveira IJ et al. Effects of Oral Vitamin C Supplementation on Anxiety in Students: A Double-Blind, Randomized, Placebo-Controlled Trial. Pak J Biol Sci. Jan 2015;18(1):11-18.
7. McCabe D et al. The impact of essential fatty acid, B vitamins, vitamin C, magnesium and zinc supplementation on stress levels in women: a systematic review. JBI Database System Rev Implement Rep. Feb 2017;15(2):402-453.
8. Leahy LG. Vitamin B Supplementation: What's the Right Choice for Your Patients? J Psychosoc Nurs Ment Health Serv. Jul 1 2017;55(7):7-11.
9. Kennedy DO. B Vitamins and the Brain: Mechanisms, Dose and Efficacy--A Review. Nutrients. Jan 27 2016;8(2):68.
10. Macpherson H et al. The Effects of Four-Week Multivitamin Supplementation on Mood in Healthy Older Women: A Randomized Controlled Trial. Evid Based Complement Alternat Med. 2016;2016:3092828.
11. Macpherson H et al. Acute mood but not cognitive improvements following administration of a single multivitamin and mineral supplement in healthy women aged 50 and above: a randomised controlled trial. Age (Dordr). Jun 2015;37(3):9782.
12. Sarris J et al. Participant experiences from chronic administration of a multivitamin versus placebo on subjective health and wellbeing: a double-blind qualitative analysis of a randomised controlled trial. Nutr J. Dec 14 2012;11:110.
13. Stough C et al. The effect of 90 day administration of a high dose vitamin B-complex on work stress. Hum Psychopharmacol. Oct 2011;26(7):470-476.
14. Long SJ et al Effects of vitamin and mineral supplementation on stress, mild psychiatric symptoms, and mood in nonclinical samples: a meta-analysis. Psychosom Med. Feb 2013;75(2):144-153.
15. Camfield DA et al. The effects of multivitamin supplementation on diurnal cortisol secretion and perceived stress. Nutrients. Nov 11 2013;5(11):4429-4450.
16. Li X et al. Effects of a multivitamin/multimineral supplement on young males with physical overtraining: a placebo-controlled, randomized, double-blinded cross-over trial. Biomed Environ Sci. Jul 2013;26(7):599-604.
17. Taylor AM et al. A review of dietary and microbial connections to depression, anxiety, and stress. Nutr Neurosci. Jul 9 2018:1-14.
18. Husted KS et al. The importance of n-6/n-3 fatty acids ratio in the major depressive disorder. Medicina (Kaunas). 2016;52(3):139-147.
19. Su KP et al. Omega-3 Polyunsaturated Fatty Acids in Prevention of Mood and Anxiety Disorders. Clin Psychopharmacol Neurosci. Aug 31 2015;13(2):129-137.
20. Thesing CS et al. Omega-3 polyunsaturated fatty acid levels and dysregulations in biological stress systems. Psychoneuroendocrinology. Nov 2018;97:206-215.
21. Fernandes MF et al. The Relationship between Fatty Acids and Different Depression-Related Brain Regions, and Their Potential Role as Biomarkers of Response to Antidepressants. Nutrients. Mar 17 2017;9(3).
22. Sauder KA et al. Effects of omega-3 fatty acid supplementation on heart rate variability at rest and during acute stress in adults with moderate hypertriglyceridemia. Psychosom Med. May 2013;75(4):382-389.
23. Barbadoro P et al. Fish oil supplementation reduces cortisol basal levels and perceived stress: a randomized, placebo-controlled trial in abstinent alcoholics. Mol Nutr Food Res. Jun 2013;57(6):1110-1114.
24. Mocking RJ et al. Fatty acid metabolism and its longitudinal relationship with the hypothalamic-pituitary-adrenal axis in major depression: Associations with prospective antidepressant response. Psychoneuroendocrinology. Sep 2015;59:1-13.
25. Kingsley M. Effects of phosphatidylserine supplementation on exercising humans. Sports Med. 2006;36(8):657-669.
26. Hellhammer J et al. A soy-based phosphatidylserine/ phosphatidic acid complex (PAS) normalizes the stress reactivity of hypothalamus-pituitary-adrenal-axis in chronically stressed male subjects: a randomized, placebo-controlled study. Lipids Health Dis. Jul 31 2014;13:121.
27. Hellhammer J et al. Effects of soy lecithin phosphatidic acid and phosphatidylserine complex (PAS) on the endocrine and psychological responses to mental stress. Stress. Jun 2004;7(2):119-126.
28. Benton D et al. The influence of phosphatidylserine supplementation on mood and heart rate when faced with an acute stressor. Nutr Neurosci. 2001;4(3):169-178.
29. Starks MA et al. The effects of phosphatidylserine on endocrine response to moderate intensity exercise. J Int Soc Sports Nutr. Jul 28 2008;5:11.
30. Porter RJ et al. Corticosteroid-serotonin interactions in depression: a review of the human evidence. Psychopharmacology (Berl). Apr 2004;173(1-2):1-17.
31. Michels N et al. Psychosocial stress and inflammation driving tryptophan breakdown in children and adolescents: A cross-sectional analysis of two cohorts. Psychoneuroendocrinology. Aug 2018;94:104-111.
32. Hood SD et al. Serotonin regulation of the human stress response. Psychoneuroendocrinology. Oct 2006;31(9):1087-1097.
33. Capello AE et al. Effect of sub chronic tryptophan supplementation on stress-induced cortisol and appetite in subjects differing in 5-HTTLPR genotype and trait neuroticism. Psychoneuroendocrinology. Jul 2014;45:96-107.
34. Cerit H et al. The effect of tryptophan on the cortisol response to social stress is modulated by the 5-HTTLPR genotype. Psychoneuroendocrinology. Feb 2013;38(2):201-208.
35. Markus CR et al. Differential effects of tri-allelic 5-HTTLPR polymorphisms in healthy subjects on mood and stress performance after tryptophan challenge. Neuropsychopharmacology. Dec 2009;34(13):2667-2674.
36. Firk C et al. Mood and cortisol responses following tryptophan-rich hydrolyzed protein and acute stress in healthy subjects with high and low cognitive reactivity to depression. Clin Nutr. Jun 2009;28(3):266-271.
37. Rea K et al. The microbiome: A key regulator of stress and neuroinflammation. Neurobiol Stress. Oct 2016;4:23-33.
38. Farzi A et al. Gut Microbiota and the Neuroendocrine System. Neurotherapeutics. Jan 2018;15(1):5-22.
39. Misra S et al. Psychobiotics: A new approach for treating mental illness? Crit Rev Food Sci Nutr. Nov 30 2017:1-7.
40. Takada M et al. Probiotic Lactobacillus casei strain Shirota relieves stress-associated symptoms by modulating the gut-brain interaction in human and animal models. Neurogastroenterol Motil. Jul 2016;28(7):1027-1036.
41. Kato-Kataoka A et al. Fermented milk containing Lactobacillus casei strain Shirota prevents the onset of physical symptoms in medical students under academic examination stress. Benef Microbes. 2016;7(2):153-156.
42. Kato-Kataoka A et al. Fermented Milk Containing Lactobacillus casei Strain Shirota Preserves the Diversity of the Gut Microbiota and Relieves Abdominal Dysfunction in Healthy Medical Students Exposed to Academic Stress. Appl Environ Microbiol. Jun 15 2016;82(12):3649-3658.
43. Andersson H et al. Oral Administration of Lactobacillus plantarum 299v Reduces Cortisol Levels in Human Saliva during Examination Induced Stress: A Randomized, Double-Blind Controlled Trial. Int J Microbiol. 2016;2016:8469018.
44. Messaoudi M et al. Assessment of psychotropic-like properties of a probiotic formulation (Lactobacillus helveticus R0052 and Bifidobacterium longum R0175) in rats and human subjects. Br J Nutr. Mar 2011;105(5):755-764.
45. Allen AP et al. Bifidobacterium longum 1714 as a translational psychobiotic: modulation of stress, electrophysiology and neurocognition in healthy volunteers. Transl Psychiatry. Nov 1 2016;6(11):e939.
46. Schmidt K et al. Prebiotic intake reduces the waking cortisol response and alters emotional bias in healthy volunteers. Psychopharmacology (Berl). May 2015;232(10):1793-1801.
47.
268. Turkozu D, Sanlier N. L-theanine, unique amino acid of tea, and its metabolism, health effects, and safety. Crit Rev Food Sci Nutr. May 24 2017;57(8):1681-1687.
269. Unno K, Tanida N, Ishii N, et al. Anti-stress effect of theanine on students during pharmacy practice: positive correlation among salivary alpha-amylase activity, trait anxiety and subjective stress. Pharmacol Biochem Behav. Oct 2013;111:128-135.
270. White DJ, de Klerk S, Woods W, Gondalia S, Noonan C, Scholey AB. Anti-Stress, Behavioural and Magnetoencephalography Effects of an L-Theanine-Based Nutrient Drink: A Randomised, Double-Blind, Placebo-Controlled, Crossover Trial. Nutrients. Jan 19 2016;8(1).
参考来源:
美国梅奥诊所
www.mayoclinic.org
美国心脏病协会
https://www.heart.org/
美国国立公众健康网
www.medlineplus.gov
美国医疗在线网
www.webmd.com
加拿大卫生部
www.hc-sc.gc.ca
免责声明和安全信息
英文名称:Chronic Stress Management,Chronic Stress,Psychological Stress
概述
现代生活中压力无处不在,每个人都时刻感觉到压力。有的压力对人体生理健康是必须的,但大部分压力尤其慢性压力却是有害的,导致如消化系统问题、头痛、失眠、情绪和心理症状等,严重的甚至可致“过劳死”。个体适应压力的能力和时间是存在差异的。维持下丘脑-垂体-肾上腺轴健康调节是防止慢性压力损害健康问题的关键之一,内分泌支持、适应原草药以及调整不良生活方式等,均可防止或改善压力带来的不利影响。什么是压力?
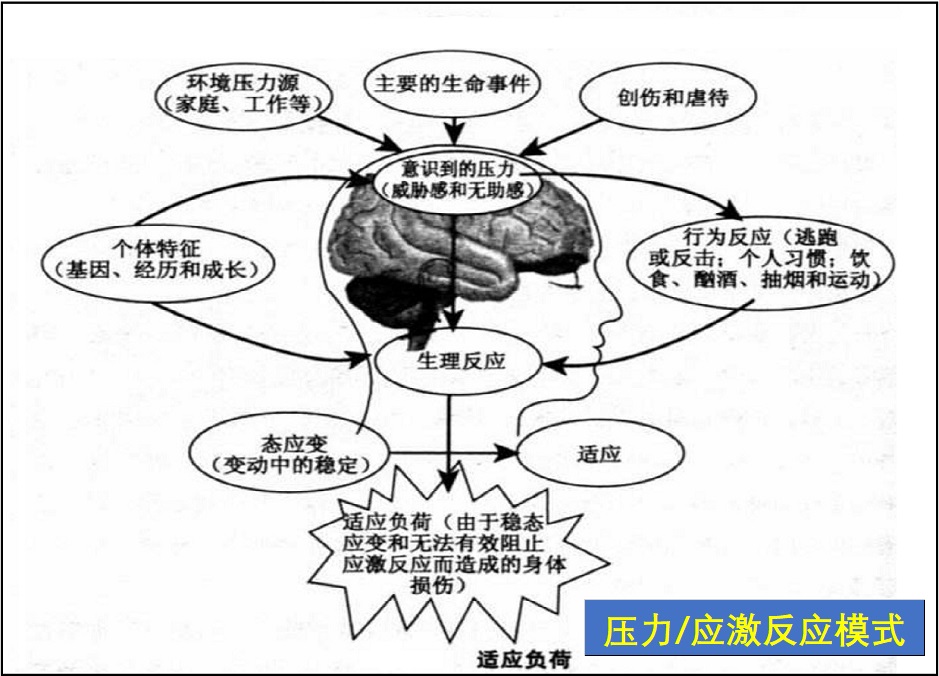
压力就是医学上所定义的应激(Stress),通常是指各种紧张性刺激物(应激源,Stressor )引起的个体非特异性反应,包括生理和心理反应。应激源是指向机体提出适应要求、并引起应对反应或稳态失衡的客观变化的环境事件或情境。应激反应分为急性和慢性2种:
- 急性应激反应:是人类适应急性刺激物进化而成的,主要表现在“战斗或逃跑反应(Fight -or-Flight Response)”,涉及的应激激素是肾上腺素,是正常的生理反应,对维持和保护机体健康是有益的和必要的。例如跑步或其他形式运动,一些令人振奋的事件或经历都是应激性压力源。
- 慢性应激反应:是由于应激源长期存在或长时间使人处于困境中而诱发的反应。这导致体内皮质醇长期处于高水平状态,因而对身心健康造成潜在危害,如胃肠失调、代谢综合征和心血管病,及精神心理疾病如焦虑、抑郁,甚至痴呆症等。
- 常规压力:与工作、家庭压力和其他日常责任相关的压力
- 突然出现负面变化所带来的压力,例如生病、失业或离婚等。
- 创伤性压力:当受到严重伤害或死亡的危险时会发生创伤性压力,包括重大事故、袭击、战争或自然灾害等,这类压力往往可导致创伤后应激障碍(PTSD)>>。
慢性压力与“过劳死”
慢性应激的后果可能是毁灭性的,已成为“过劳死、猝死”的主要诱发因素。研究表明,慢性应激是导致压力性/应激性心肌病(Stressful/Takotsubo Cardiomyopathy)或心碎症候群(Broken Heart Syndrome)的最主要因素之一。应激性心肌病是一种自发性的心脏衰弱,使患者容易发生心律失常,甚至心脏性猝死。虽然机制尚不清楚,但一般认为慢性应激引起的肾上腺素过度升高刺激心肌,以及改变其功能并引起心房重塑等有关。
- 长期压力与炎症循环标志物升高和内膜中层厚度增加有关,这是动脉粥样硬化进展的一种指标。
- 慢性压力通过引起大脑的结构和功能变化,大大增加了焦虑和抑郁的风险。
- 缺乏适当的压力管理和适应慢性压力的男性群体更有可能超重,及发展性功能障碍。
人。点击了解更多相关内容: 心碎症候群 >>
慢性应激发生机制
慢性压力的核心是下丘脑-垂体-肾上腺轴(HPA)的失调,这是一个生理指令调节的回馈网络,负责控制皮质醇和儿茶酚胺(如肾上腺素和去甲肾上腺素)等应激激素的产生。慢性压力导致HPA轴的不同步以及随后的压力激素水平失衡,这是压力相关疾病的一个关键特征。1.身体对压力的反应
当个体经历身体或精神、内源或环境等压力源时,机体将启动复杂的适应性压力系统。这种反应过程导致肾上腺应激激素(即糖皮质激素)和儿茶酚胺的释放,以刺激身体有关系统的适应性变化。
2.“战斗或逃跑”应激反应
- 在短期情况下,应激诱导的变化优先考虑逃避危险的功能,从其他多数的身体部位改变血液流向肌肉,增加血压和血糖水平、瞳孔扩张,以及抑制消化以节约能量。在此期间,脂肪酸和葡萄糖(血糖)从储存部位释放到血流中,在那里它们变得容易被肌肉利用。这就是所谓的“战斗或逃跑”应激反应。这种反应和适应性保护系统起源于大脑。
- 在感知到压力后,下丘脑中的特化神经元通过释放促肾上腺皮质激素释放激素(CRH)和血管加压素(VP)等响应而作出反应。随后,这些激素刺激垂体腺释放促肾上腺皮质激素(ACTH)。
- 进入血液循环并到达肾上腺后,ACTH刺激糖皮质激素和儿茶酚胺的产生,然后儿茶酚胺作用于整个身体,以诱导适应性变化。这种脑-内分泌协调包括下丘脑-垂体-肾上腺轴(HPA)调节作用。
- 虽然战斗或逃跑的反应无疑是必要的,以便在紧急情况下对即将发生的危险做出自主反应。现代人生活在充满压力的环境中,包括经济担忧,以及学校、工作的最后期限等压力。所有这些应激都以一种进化上不自然的方式长期激活HPA轴,导致压力激素水平持续升高,引起全天候的生理变化。
- 这对机体健康是极为有害的,例如造成胰岛素抵抗和血压升高,以及其他一些与压力相关的生理缺陷等,导致多种慢性病。
- 糖皮质激素(应激激素)水平的慢性长期升高损害并破坏负责调节CRH释放的下丘脑区域的神经元。这导致HPA轴反应不稳定或不足,因而可能导致心理障碍,例如抑郁和焦虑等。
3.了解皮质醇作用:皮质醇是肾上腺分泌的最主要应激激素。适量的皮质醇是维持最佳健康所必需的,但过多或过少都可造成损害。其主要功能是:
- 通过肝脏中的糖异生过程调节血糖水平
- 对免疫系统调节
- 调节代谢碳水化合物、蛋白质和脂质
- 皮质醇受体在整个机体中表达,包括在大脑中。因此,皮质醇的合成、代谢和释放的紊乱可以破坏许多生理系统而造成健康问题。
- 皮质醇是一种分解代谢激素,当失去平衡和失控时,可对身体产生不利影响,例如:过多的皮质醇可以抑制免疫系统,而过少则可导致自体免疫疾病。这是许多疾病产生的根源。
- 皮质醇生物合成和释放的复杂过程对内部和外部因素的破坏敏感,如面对慢性心理压力,肾上腺在异常节律中排出异常量的皮质醇。
- 在身体健康情况下,皮质醇水平在早上8点左右达到峰值;在午夜和凌晨4点之间下降到最低点。经常熬夜或睡眠不佳者,却破坏了这一生理平衡规律。
4.认知机体对压力反应过程
研究表明,每个人天生适应压力能力是不同的。然而,耐受性是可变的,因为一些人只能处理低水平和短持续时间的压力,而另一些人则可以在更长时间内适应更高水平的压力。1935年,美国H. Selye博士提出了压力/应激概念,并指出在处理压力时身体会面临三种状态:
- 早期的警报状态:适应急性应激,即 “战斗或逃跑”反应。
- 身体试图适应增加抗压(皮质醇释放)的抵抗状态,即长期应激反应激活,胰岛素抵抗后果出现。
- 压力压倒和削弱机体系统后的疲劳状态:HPA轴的相应性和敏感性下降,即下丘脑-垂体功能障碍,导致不稳定/不足的应激激素和儿茶酚胺产生,以及随之而来的情绪障碍和慢性疲劳等。
附注:关于“肾上腺疲劳(Adrenal Fatigue)问题:
“肾上腺疲劳”是涉及压力问题的替代医学常用术语,虽然还没有得到传统医学的公认诊断。“肾上腺疲劳”的症状是由多因素病理过程引起的,其中包括HPA轴。
此外,艾迪生病或称为“肾上腺皮质功能不全”,是一种可能危及生命的疾病。它主要是自体免疫性疾病的结果,但也可能由遗传异常引起。艾迪生病比压力引起的后果更为严重,应由合格的医疗专业人员密切监测、诊断和治疗。
慢性应激症状
容易忽略的是压力对健康存在多方面的影响。头痛、经常失眠或工作效率下降等,压力症状不但影响身体,还包括思想、感觉认知以及行为等。而长期压力结果可导致高血压、心脏病、肥胖和糖尿病,以及抑郁甚至痴呆等系列健康问题。与慢性压力有关的症状常见如下:
- 表现在身体上包括:
- 头痛
- 肌肉紧张或疼痛
- 胸部不适
- 性欲变化
- 经前综合征
- 生殖能力下降
- 疲劳,有时感觉虚弱
- 睡眠问题
- 慢性过敏,免疫失衡
- 胃肠不适
- 慢性低血压
- 表现在精神或情绪上如:
- 焦虑
- 心神不定、坐立不安
- 思维缓慢,记忆下降
- 经常感到不知所措
- 烦躁、易怒
- 情绪低落或抑郁
- 对日常行为的影响,如
- 暴饮暴食或过度劳累
- 依赖咖啡
- 易怒
- 酒精或药物滥用
- 渴望糖或咸的食物
- 吸烟多
- 社交萎缩
- 对冷敏感,怕冷
- 不愿运动锻炼
疗法
综合治疗最有效,选项可包括如下:调整饮食与生活方式
- 健康饮食,富含新鲜蔬菜、水果和全谷类食物,以及深海鱼、坚果等
- 适度饮酒,尤其晚餐不宜饮酒
- 不要抽烟,或戒烟
- 限制咖啡因,晚餐后不宜饮用
- 良好、充足睡眠
- 经常运动锻炼
- 学会和运用放松技巧,如深呼吸、冥想、瑜伽和按摩等
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于慢性应激管理的营养和草本补充剂,主要包括如下:
1. 维生素C:
肾上腺具有体内最高浓度的维生素C1。除了其众所周知的自由基清除剂功能外,维生素C还是儿茶酚胺合成的辅助因子,儿茶酚胺是参与应激反应的神经激素,有助于调节中枢神经系统的活动1-3。在应激或感染期间,血液和白细胞中的维生素C水平会迅速下降4,而抑郁和焦虑症状与维生素C的低摄入和低循环水平有关2。
在一项对照临床试验中,压力诱导的焦虑和抑郁患者的维生素C以及维生素E和A水平低于健康受试者,与单独的抗抑郁治疗相比,在抗抑郁治疗中添加这些营养素维生素C、维生素E和β-胡萝卜素(维生素A)可以更大程度地减轻焦虑和抑郁症状5。另一项对照试验发现,在健康的高中生中,每天补充500mg维生素C可以减少焦虑水平,降低平均心率6。此外,一项研究综述表明,高剂量的维生素C可以减轻焦虑,缓解与压力相关的血压升高7。
2. 维生素B族与复合维矿素:
B族维生素缺乏与神经精神疾病有关,如抑郁症、阿尔茨海默病、精神分裂症和其他类型的精神病和痴呆症,健康的神经系统功能需要充足的所有B族维生素8,9。
多种维生素减轻压力和疲劳的能力已经在许多试验中得到证实10-12。在一项针对60名工作成年人的随机对照试验中,那些连续12周每天服用高剂量复合B族维生素的人与服用安慰剂的人相比,压力、困惑和抑郁情绪水平较低13。一项研究综述得出结论,复合维生素,特别是复合维生素B补充剂,可以有效地降低感知压力,减轻轻度精神症状,改善健康个体的日常情绪14。
B族维生素也可以支持正常的HPA轴功能。在一项有138名受试者参与的安慰剂对照试验中,补充含有B族维生素的复合维矿素16周后,皮质醇唤醒反应增强。皮质醇觉醒反应发生在醒来后约30分钟,通常导致一天中最高的皮质醇水平,被认为是健康的下丘脑轴张力的标志,并且与一天中其余时间较低的痛苦水平有关15。另一项随机对照交叉试验检测了240名承受剧烈身体压力的中国军人服用一周复合维生素补充剂的效果。复合维生素与正常下丘脑轴功能的更好恢复和心理症状的改善有关16。
3. 欧米伽3脂肪酸:
ω-3脂肪酸(EPA和DHA)可能有助于预防和治疗压力、焦虑和抑郁17-19。血液中EPA和DHA的低水平与压力的几个生物学指标有关:炎症标志物升高、神经系统信号传导失调和HPA轴高活性20,21。相反,ω-6脂肪酸主要通过食用动物脂肪和加工植物油获得,可促进炎症,从而诱导应激信号,并导致应激相关疾病18。
在一项针对甘油三酯水平高的参与者的随机对照试验中,连续八周服用3400mg EPA和DHA会增加心率变异性,表明与压力相关的神经系统信号较低;然而,每天850mg的较低剂量没有效果22。另一项对照试验发现,在住院治疗计划中,每天60mg EPA和252mg DHA的三周治疗改善了酒精受试者的压力和焦虑,并降低了皮质醇水平23。抑郁症患者的试验证据表明,ω-3脂肪酸可以纠正HPA过动,减轻症状,并可能提高对抗抑郁治疗的反应性21,24。
4.丝氨酸磷脂:
磷脂酰丝氨酸存在于细胞膜中,有助于促进健康的细胞通讯。它调节组织对炎症的反应,并可以减少氧化应激25。多项研究表明,丝氨酸磷脂可以平衡HPA轴信号传导,并可能限制肾上腺过度激活的负面后果。
在一项针对75名健康男性志愿者的试验中,在报告慢性压力水平高的男性亚群中,服用每组提供400mg磷脂酰丝氨酸及其前体磷脂酸的补充剂42天,降低了HPA轴对急性压力的反应26。在其他临床研究中,同样的组合被注意到可以减轻对精神压力的应激反应27。而每天单独服用300mg磷脂酰丝氨酸可以减少感知到的压力,改善容易产生焦虑、担心和恐惧等健康年轻人的情绪28。磷脂酰丝氨酸也被发现可以降低皮质醇水平,降低男性急性运动时的皮质醇反应,这种效果可能有助于防止过度训练的有害后果,如表现下降、受伤、免疫抑制和心理健康的恶化29。
5. 色氨酸:
L-色氨酸是神经递质血清素的一种氨基酸前体。血清素与应激反应有着复杂的关系30。应激性炎症似乎会导致色氨酸的过度分解,这可能会减少血清素的产生,增加抑郁的风险31;此外,色氨酸耗竭已被证明可增加应激敏感性32。
对健康成人的研究表明,每天补充800到2800mg的色氨酸,可降低皮质醇对压力的反应,减轻与压力相关的负面情绪,并防止一些人的压力性进食33-35。在一项随机对照试验中,富含色氨酸的水解蛋白补充剂在急性应激反应中增加积极情绪并降低皮质醇释放36。
6.益生菌和益生元:
肠道微生物组、神经系统和HPA轴紧密相关。益生菌和益生元可以改善肠道细菌的平衡,越来越多的证据表明,它们有可能对压力反应产生积极影响17,36,38。研究表明,益生菌可以降低压力反应性和焦虑,改善情绪、记忆力和认知,导致一些研究人员将具有这些作用的益生菌称为“心理益生菌(Psychobiotics)”39。
在几项试验中发现,用干酪乳杆菌菌株Shirota(代田菌)制成的发酵乳制品可以抑制皮质醇在压力下的升高,并减少健康医学生的压力相关健康问题,如抑郁或焦虑情绪、消化不良和感冒症状40-42。在一项随机对照试验中,每天补充100亿CFU 植物乳杆菌299v、连续10天,可降低即将进行检查的学生的唾液皮质醇水平43。在其他对照试验中,以每天30亿CFU的剂量服用瑞士乳杆菌R0052和长双歧杆菌R0175(Lallemand益生菌专有品牌CEREBIOME®)的组合,在30天的时间里,健康志愿者的感知压力和尿皮质醇水平的评分降低了44,并且在四周内每天补充10亿CFU的长双歧杆菌菌株1714抑制了皮质醇的升高和与急性压力相关的主观焦虑45。
益生元在临床研究中也显示出积极作用:在一项针对45名健康成年人的试验中,连续三周服用5.5g含有低聚半乳糖的益生元补充剂,可降低清晨皮质醇水平,并更平衡地处理积极和消极的情绪刺激46。
7.茶氨酸:
L-茶氨酸具有抗应激作用。大量研究发现,茶和茶氨酸可以降低感知到的压力和压力反应的生理标志物,包括血压、心率、皮质醇水平和大脑活动模式47。在一项包括20名药学学生的试验中,一周内每天两次服用200mg茶氨酸,比安慰剂更能降低早晨唾液α-淀粉酶水平。此外,服用L-茶氨酸的受试者报告的主观压力明显低于安慰剂组48。
L -茶氨酸的短期效果在另一项随机对照试验中得到证实,该试验有36名年龄在18至40岁之间的健康参与者参加:单次200mg剂量的茶氨酸在给药后一小时降低了主观压力,在给药后三小时降低了对认知压力源的皮质醇反应。此外,在焦虑倾向测试中得分较高的一部分参与者中,茶氨酸增加了与放松相关的脑电波活动49。
日本研究人员进行的一系列小型试验发现,在实验室进行的应激算术测试中,补充L-茶氨酸可以防止心率升高。服用L-茶氨酸的人,在应对应激任务时,唾液免疫球蛋白A(s-IgA)水平也会降低。研究人员得出结论,服用L-茶氨酸的受试者心率和s-IgA的降低可能归因于交感神经系统活动的减弱50。
茶氨酸还被证明可以对抗咖啡因的压力诱导作用,增强集中注意力51。一项为期两个月的临床试验指出,茶氨酸与维生素/矿物质/草药补充剂相结合,可以降低老年人的感知压力评分,改善认知功能52。
8. γ-氨基丁酸:可改善α脑电波、激活副交感神经,具有醒脑和安神促进睡眠等作用,可增强日常有关的抗压能力53,54,并改善认知功能。
注意:普通γ氨基丁酸是合成的,效果不如预期,而且作用一直存在争议。通过发酵产生的成分—γ氨基丁酸PharmaGABA®,被证实效果好且安全。
9.褪黑素:
褪黑激素与睡眠周期的关系众所周知。褪黑素在包括HPA轴在内的身体系统的昼夜节律调节中发挥着核心作用55。压力会降低褪黑激素水平并破坏身体的生物节律56。大脑内部时钟的慢性破坏,如轮班工作或失眠,会损害身心健康57,58。
补充褪黑激素可以改善睡眠量和质量,有助于恢复正常的昼夜节律59,60,这可能会减轻压力,防止与压力相关的健康恶化61。在一项研究中,在一组老年女性志愿者中,在晚上服用2mg褪黑素六个月,可以改善睡眠,提高循环的DHEA-S水平62。
10.脱氢表雄酮:
脱氢表雄酮(DHEA)是一种肾上腺激素,与皮质醇一样,它是在急性压力时分泌的,但慢性压力与低水平有关63。压力对DHEA的影响可能是将压力与健康不佳和衰老加速联系起来的因素之一64。低DHEA-S水平与骨质疏松、认知能力下降和痴呆等疾病有关,以及心血管疾病、情绪障碍和性功能障碍65。临床前和临床研究结果表明,DHEA替代疗法可能在保护衰老的骨骼和血管系统方面发挥作用,并可能有助于治疗抑郁症和性障碍65,66。
在一项随机、安慰剂对照、交叉试验中,年龄在40岁至70岁之间的13名男性和17名女性接受了为期6个月的每日50mg DHEA治疗,身体和心理健康状况显著改善67。在另一项研究中,24名健康的年轻男性服用了高剂量DHEA(每天两次,每次150mg),为期7天。受试者报告情绪有所改善,DHEA治疗导致夜间皮质醇水平降低68。
DHEA的补充剂量通常为女性每天10-25 mg,男性每天25-75 mg,但应基于DHEA-S血液水平检测。了解更多相关内容,可参阅本网站相关专文:DHEA与抗衰老 >>
11.镁:
镁是一种重要的矿物质,在数百个生物化学过程中起辅助因子的作用,包括那些参与应激反应的过程。镁可以抑制谷氨酸受体,减弱兴奋性传递,促进GABA和血清素活性69。临床前和临床研究观察到,镁水平受到应激刺激的负面影响,补充镁可以减轻压力70,71。镁水平低会进一步加剧压力,因为镁间接减少皮质醇分泌69。
研究表明,苏糖酸镁比普通镁制剂可更有效地提高脑内镁水平。此外,乙酰牛磺酸镁是一种镁的有机盐,与其他形式的镁相比,它在大脑中的生物利用度有所提高72。
12.姜黄素:
作为一种多酚,姜黄素具有很强的自由基猝灭和抗炎作用。阿育吠陀医学使用其治疗一系列炎症性疾病,包括肌肉骨骼问题、神经系统疾病、心脏病73。许多临床研究表明,姜黄素有可能减少慢性和重复压力对认知功能和情绪的影响74-77。此外,临床前证据表明,姜黄素的抗应激作用可能与其减少神经炎症和保持神经可塑性的能力有关78-80。
多项随机对照试验和三项荟萃分析表明,姜黄素可以减轻抑郁症患者的抑郁和焦虑症状81-83。一项针对60名患有职业压力相关焦虑症的参与者的临床试验,将高吸收姜黄素加胡芦巴的组合(每天1000mg)与相同剂量的标准姜黄素或安慰剂进行了比较。30天后,与服用普通姜黄素或安慰剂的参与者相比,服用姜黄素/胡芦巴组合的参与者报告压力、焦虑和疲劳减轻得更多,生活质量也得到了更大的改善84。在另一项针对80名糖尿病神经病变参与者的安慰剂对照试验中,与安慰剂相比,每天服用80mg不同的高吸收形式的姜黄素、持续8周可降低抑郁和焦虑症状评分85。在重度抑郁障碍患者中,与服用安慰剂的患者相比,每天摄入1500mg姜黄素12周的患者抑郁症状改善更大。此外,在试验结束四周后,这种益处仍然是可以测量的86。在耐力训练期间,补充姜黄素也被发现比安慰剂更好地降低运动员的感知压力水平87。
13. 厚朴和黄柏:
厚朴的活性成分厚朴酚等在临床前和临床试验中被发现具有多种有益作用,包括减轻应激88。在暴露于慢性应激的啮齿类动物中,厚朴酚等组合被发现可以使血清素和HPA轴活性正常化,增加大脑生长因子(脑源性神经营养因子,BDNF)的水平,减少神经炎症和大脑氧化应激,并预防抑郁行为89-92。
厚朴和黄柏的组合也被研究用于抗应激作用。在一项对照临床试验中,56名中等压力水平的健康受试者接受了提供250mg厚朴和黄柏补充剂或安慰剂,每天两次,持续四周。参与者接受了三次(上午、中午和晚上)唾液皮质醇测试,并在试验开始和结束时回答了情绪问卷。与安慰剂组相比,接受补充剂组的皮质醇总暴露量较低,情绪评分较好93。
研究了相同的组合补充剂对应激诱导的食欲和体重增加的影响。在一项对照试验中,与安慰剂相比,厚朴加黄柏剂量为250 mg,每天三次、持续六周,减轻了超重但健康的绝经前女性的体重增加,这些女性报告称饮食压力大,焦虑水平高于平均水平94。在另一项类似设计的试验中,厚朴和黄柏减轻了暂时的焦虑,但对长期抑郁或焦虑、食欲、睡眠或唾液皮质醇和淀粉酶水平没有影响95。
14.适应原药草:
适应原药草(Adaptogenic herbs)具有多方面的有益作用,支持身体对压力条件的内在弹性。它们通过以支持体内平衡的方式调节生物网络来发挥作用。例如,适应原可以提高能量水平,但也支持健全的睡眠。使用适应原的一些典型益处包括缓解疲劳、改善认知功能和情绪以及支持免疫系统等96-98。
- 南非醉茄:阿育吠陀医学的重要草药之一,常作为补品和春药99。大量临床前研究表明,南非醉茄(或印度人参)可以防止氧化损伤,支持正常的线粒体活性,调节中枢神经系统信号传导,并有助于免疫调节,提示它可能用于治疗慢性应激相关、炎症、代谢、心血管和神经退行性疾病100-102。
一些临床试验进一步表明,南非醉茄对缓解压力和焦虑有效103。例如,在一项有64名参与者的试验中,治疗60天后,每天两次的300mg 南非醉茄提取物在降低感知压力评分和降低血液皮质醇水平方面比安慰剂更有效104。另一项试验指出,南非醉茄可能对慢性压力患者的体重管理产生有益影响。52名慢性应激参与者接受每天两次300mg 南非醉茄或安慰剂治疗,持续8周;南非醉茄治疗组比安慰剂组在感知压力和血清皮质醇水平方面有更大的降低,在食物渴望和饮食行为方面有更多的改善,体重减轻幅度更大105。
- 红景天:一种主要生长在北极地区的适应性草本植物,一般被用于增强身心耐力和缓解压力106。红景天似乎可以调节HPA轴功能,减少氧化应激,并调节免疫活性107,108。
在有慢性疲劳症状、倦怠和轻度焦虑的患者中进行的试点试验发现,每天400mg红景天提取物与能量水平、情绪、睡眠、认知功能的改善有关109-111;红景天也被发现可以帮助压力诱导的抑郁症患者112。这种效果可能部分是由于它促进了大脑中的新连接113。
- 人参:包括亚洲参、西洋参。其活性成分—人参皂苷因其对疾病预防和整体健康的影响而被广泛研究114。人参功能作用包括如:抗应激反应、免疫调节、抗炎、抗癌、清除自由基,以及对神经和心脏保护等115-118。关于应激生理学,发酵人参提取物被发现可以减少对运动应激的氧化应激和HPA轴信号传导119。
- 刺五加:源自西伯利亚的一种流行的适应原草本植物。它含有一种名为刺五加苷的活性化合物,并具有一系列抗应力性能120。
- 五味子:一种传统药草,被用于治疗精神症状和失眠,以及与疲劳和虚弱有关的各种健康问题121,122。五味子及其活性成分还表现出护肝、抗炎、免疫调节、抗增殖和增强认知的作用。五味子也有望成为心脏和神经保护剂121-123。动物研究结果表明,五味子可能有助于调节HPA轴活性,缓解压力的负面影响124-126。
- 冬虫夏草:在传统中医中用于治疗疲劳,并作为健康、长寿和身体机能的促进剂127,128。已经鉴定出冬虫夏虫夏草中的许多活性化合物,研究表明它们具有抗炎、免疫调节和减少氧化应激的作用129。此外,临床前研究表明,虫草具有抗衰老、抗疲劳、神经保护和壮阳的潜力128。在慢性应激的动物模型中,补充虫草可以缓解由不可预测和反复的轻度应激引起的抑郁样行为。此外,虫草治疗降低了一些炎症标志物,并上调了BDNF的表达130。初步临床证据表明,虫草可以改善运动表现,抑制运动诱导的皮质醇释放增加,这可能有助于预防过度训练的有害影响131。
- 余柑子(印度醋栗):在阿育吠陀医学中用于恢复力量和健康132。其所含的一些活性成分已显示出强大的氧化应激降低能力133。在12名健康志愿者的初步试验中,500mg标准化余柑子提取物,每天两次,持续14天,缓解了急性应激引起的动脉硬化增加和心血流量减少134。对动物的研究表明,印度醋栗可以减少大脑氧化应激,防止对睾丸组织的慢性应激相关损伤,总体上提高应激弹性以及延长寿命135-137。
- 圣罗勒:阿育吠陀传统中的一种适应性草本植物138。许多临床和临床前研究已经证明了圣罗勒的抗压力潜力,因为它被证明可以改善情绪和认知,使新陈代谢正常化,调节免疫功能,减少氧化应激,并通过支持解毒来防止各种组织的毒性损伤138,139。
在一项有40名参与者的随机对照试验中,与安慰剂相比,每天服用300mg圣罗勒提取物,持续30天,减轻了焦虑症状,提高了认知测试分数140。另一项随机对照试验的结果表明,150名参与者每天服用1200mg圣罗勒或安慰剂,圣罗勒可以减轻与压力相关的症状,如焦虑、疲劳、睡眠困难和性功能障碍141。在一项试验性试验中,35名焦虑症患者每天两次接受500mg圣罗勒治疗,结果发现治疗可减轻焦虑、压力和抑郁症状142。
15.假马齿苋:在阿育吠陀医学中历来被用于支持健康的认知功能143。许多动物研究已经证明了它的适应性潜力,指出它能够使应激激素水平和神经递质平衡正常化144,减少氧化应激145,防止神经退行性变146,并预防或逆转应激的其他负面生理和行为后果147-149。此外,在慢性应激的啮齿动物模型中,已经发现假马齿苋和一种活性成分(假马齿苋皂苷I)可以减少抑郁行为,使HPA轴功能正常化,减少脑氧化应激,并防止BDNF的下降和大脑环境中的其他变化150-152。在另一个实验室动物模型中,巴科帕也被发现可以提高应激能力和寿命153。
在一项针对17名健康成年人的初步试验中,假马齿苋标准化提取物,单剂量320mg和640mg,在一到两小时后的多任务心理测试中改善了认知表现,同时也降低了皮质醇水平,这表明其认知益处的一部分可能与减压效果有关154。在一项对54名老年受试者的随机对照试验中,与安慰剂相比,每天300mg的假马齿苋持续12周可改善认知能力,降低抑郁和焦虑评分,并降低心率155。
16.藏红花:藏红花是一种药食同源的药草,具有镇静、适应和其他特性。几项临床试验表明,藏红花有助于治疗轻度至中度抑郁症156,157。藏红花及其活性成分番红花素在动物研究中也显示出抗应激和抗焦虑的作用,临床前证据表明,它可能部分通过调节HPA轴反应来发挥其益处158-161。此外,另一种来自藏红花的活性化合物被发现可以预防大鼠应激诱导的抑郁行为162。
在一项随机对照试验中,没有抑郁症但报告情绪低落的受试者接受了为期四周的每天28mg藏红花提取物的治疗,与接受安慰剂治疗的人相比,他们的情绪得到了更大的改善,压力和焦虑症状也得到了减轻163。
17. 香蜂草:植物薄荷科家族成员之一,既是食用香料,作为草药可放松和振奋神经系统164,165。在食物或饮料中食用发现,香蜂草通常能改善健康年轻成年人的情绪和认知表现166。在暴露于实验压力的健康受试者中,个别剂量的香蜂草具有急性抗应激和增强认知的作用,并提高了自我报告的平静和警觉167。
在一项针对20名轻度至中度焦虑和失眠的压力志愿者的试点试验中,19名(95%)参与者每天两次用300mg香蜂草提取物治疗15天,症状得到改善。此外,14名参与者的焦虑完全缓解,17人失眠缓解,14人焦虑和失眠都得到缓解168。在一项针对80名稳定型心绞痛患者的安慰剂对照临床试验中,每天3g香蜂草提取物持续8周,可以减轻焦虑、抑郁和压力,改善睡眠169。在动物研究中,香蜂草减轻了应激引起的肠易激综合征症状170。
更多内容可点击其个性化的综合干预方案如下:
- 慢性压力管理要略:
- 慢性压力管理(调节内稳态)
- 慢性压力管理(增强抗压)
- 慢性压力管理(抗紧张焦虑)
- 慢性压力管理(增加耐力)
- 慢性压力管理(滋补脑神经)
- 慢性压力管理(改善脑分泌)
- 慢性压力管理(舒缓脑神经)
- 慢性压力管理(调节皮质醇)
- 慢性压力管理(睡眠抗压)
- 精神压力缓解:
以及参阅本网如下专文的相关内容:
医疗干预
常规治疗:主要使用精神类药物治疗压力失衡引起的症状。但无法解决与压力有关的生化异常,如肾上腺激素紊乱等。
预防
没有预防慢性应激的指南。然而,采取下列措施有助于减少压力的发生或其负面作用:
- 定期进行身体活动、锻炼,尤其有氧运动、徒步旅行。
- 学会和运用各种放松技巧,如:冥想、正念思维、瑜伽、按摩和深呼吸等。
- 与家人、朋友交往。
- 听音乐、读书。
- 专注爱好。
- 幽默。
- 临床验证的替代疗法、营养和草药等。
- 养宠物,如狗、猫。研究表明,这有助于缓解压力。
- 不宜长时间看电视、上网或玩视频游戏。
- 充足、良好睡眠。
- 限制酒精、咖啡饮料。
参考文献:
1. Figueroa-Méndez R et al. Vitamin C in Health and Disease: Its Role in the Metabolism of Cells and Redox State in the Brain. Front Physiol. 2015;6:397.
2. Kocot J et al. Does Vitamin C Influence Neurodegenerative Diseases and Psychiatric Disorders? Nutrients. Jun 27 2017;9(7).
3. Han QQ et al. Preventive and Therapeutic Potential of Vitamin C in Mental Disorders. Curr Med Sci. Feb 2018;38(1):1-10.
4. Chambial S et al. Vitamin C in disease prevention and cure: an overview. Indian J Clin Biochem. Oct 2013;28(4):314-328.
5. Gautam M et al. Role of antioxidants in generalised anxiety disorder and depression. Indian J Psychiatry. Jul 2012;54(3):244-247.
6. De Oliveira IJ et al. Effects of Oral Vitamin C Supplementation on Anxiety in Students: A Double-Blind, Randomized, Placebo-Controlled Trial. Pak J Biol Sci. Jan 2015;18(1):11-18.
7. McCabe D et al. The impact of essential fatty acid, B vitamins, vitamin C, magnesium and zinc supplementation on stress levels in women: a systematic review. JBI Database System Rev Implement Rep. Feb 2017;15(2):402-453.
8. Leahy LG. Vitamin B Supplementation: What's the Right Choice for Your Patients? J Psychosoc Nurs Ment Health Serv. Jul 1 2017;55(7):7-11.
9. Kennedy DO. B Vitamins and the Brain: Mechanisms, Dose and Efficacy--A Review. Nutrients. Jan 27 2016;8(2):68.
10. Macpherson H et al. The Effects of Four-Week Multivitamin Supplementation on Mood in Healthy Older Women: A Randomized Controlled Trial. Evid Based Complement Alternat Med. 2016;2016:3092828.
11. Macpherson H et al. Acute mood but not cognitive improvements following administration of a single multivitamin and mineral supplement in healthy women aged 50 and above: a randomised controlled trial. Age (Dordr). Jun 2015;37(3):9782.
12. Sarris J et al. Participant experiences from chronic administration of a multivitamin versus placebo on subjective health and wellbeing: a double-blind qualitative analysis of a randomised controlled trial. Nutr J. Dec 14 2012;11:110.
13. Stough C et al. The effect of 90 day administration of a high dose vitamin B-complex on work stress. Hum Psychopharmacol. Oct 2011;26(7):470-476.
14. Long SJ et al Effects of vitamin and mineral supplementation on stress, mild psychiatric symptoms, and mood in nonclinical samples: a meta-analysis. Psychosom Med. Feb 2013;75(2):144-153.
15. Camfield DA et al. The effects of multivitamin supplementation on diurnal cortisol secretion and perceived stress. Nutrients. Nov 11 2013;5(11):4429-4450.
16. Li X et al. Effects of a multivitamin/multimineral supplement on young males with physical overtraining: a placebo-controlled, randomized, double-blinded cross-over trial. Biomed Environ Sci. Jul 2013;26(7):599-604.
17. Taylor AM et al. A review of dietary and microbial connections to depression, anxiety, and stress. Nutr Neurosci. Jul 9 2018:1-14.
18. Husted KS et al. The importance of n-6/n-3 fatty acids ratio in the major depressive disorder. Medicina (Kaunas). 2016;52(3):139-147.
19. Su KP et al. Omega-3 Polyunsaturated Fatty Acids in Prevention of Mood and Anxiety Disorders. Clin Psychopharmacol Neurosci. Aug 31 2015;13(2):129-137.
20. Thesing CS et al. Omega-3 polyunsaturated fatty acid levels and dysregulations in biological stress systems. Psychoneuroendocrinology. Nov 2018;97:206-215.
21. Fernandes MF et al. The Relationship between Fatty Acids and Different Depression-Related Brain Regions, and Their Potential Role as Biomarkers of Response to Antidepressants. Nutrients. Mar 17 2017;9(3).
22. Sauder KA et al. Effects of omega-3 fatty acid supplementation on heart rate variability at rest and during acute stress in adults with moderate hypertriglyceridemia. Psychosom Med. May 2013;75(4):382-389.
23. Barbadoro P et al. Fish oil supplementation reduces cortisol basal levels and perceived stress: a randomized, placebo-controlled trial in abstinent alcoholics. Mol Nutr Food Res. Jun 2013;57(6):1110-1114.
24. Mocking RJ et al. Fatty acid metabolism and its longitudinal relationship with the hypothalamic-pituitary-adrenal axis in major depression: Associations with prospective antidepressant response. Psychoneuroendocrinology. Sep 2015;59:1-13.
25. Kingsley M. Effects of phosphatidylserine supplementation on exercising humans. Sports Med. 2006;36(8):657-669.
26. Hellhammer J et al. A soy-based phosphatidylserine/ phosphatidic acid complex (PAS) normalizes the stress reactivity of hypothalamus-pituitary-adrenal-axis in chronically stressed male subjects: a randomized, placebo-controlled study. Lipids Health Dis. Jul 31 2014;13:121.
27. Hellhammer J et al. Effects of soy lecithin phosphatidic acid and phosphatidylserine complex (PAS) on the endocrine and psychological responses to mental stress. Stress. Jun 2004;7(2):119-126.
28. Benton D et al. The influence of phosphatidylserine supplementation on mood and heart rate when faced with an acute stressor. Nutr Neurosci. 2001;4(3):169-178.
29. Starks MA et al. The effects of phosphatidylserine on endocrine response to moderate intensity exercise. J Int Soc Sports Nutr. Jul 28 2008;5:11.
30. Porter RJ et al. Corticosteroid-serotonin interactions in depression: a review of the human evidence. Psychopharmacology (Berl). Apr 2004;173(1-2):1-17.
31. Michels N et al. Psychosocial stress and inflammation driving tryptophan breakdown in children and adolescents: A cross-sectional analysis of two cohorts. Psychoneuroendocrinology. Aug 2018;94:104-111.
32. Hood SD et al. Serotonin regulation of the human stress response. Psychoneuroendocrinology. Oct 2006;31(9):1087-1097.
33. Capello AE et al. Effect of sub chronic tryptophan supplementation on stress-induced cortisol and appetite in subjects differing in 5-HTTLPR genotype and trait neuroticism. Psychoneuroendocrinology. Jul 2014;45:96-107.
34. Cerit H et al. The effect of tryptophan on the cortisol response to social stress is modulated by the 5-HTTLPR genotype. Psychoneuroendocrinology. Feb 2013;38(2):201-208.
35. Markus CR et al. Differential effects of tri-allelic 5-HTTLPR polymorphisms in healthy subjects on mood and stress performance after tryptophan challenge. Neuropsychopharmacology. Dec 2009;34(13):2667-2674.
36. Firk C et al. Mood and cortisol responses following tryptophan-rich hydrolyzed protein and acute stress in healthy subjects with high and low cognitive reactivity to depression. Clin Nutr. Jun 2009;28(3):266-271.
37. Rea K et al. The microbiome: A key regulator of stress and neuroinflammation. Neurobiol Stress. Oct 2016;4:23-33.
38. Farzi A et al. Gut Microbiota and the Neuroendocrine System. Neurotherapeutics. Jan 2018;15(1):5-22.
39. Misra S et al. Psychobiotics: A new approach for treating mental illness? Crit Rev Food Sci Nutr. Nov 30 2017:1-7.
40. Takada M et al. Probiotic Lactobacillus casei strain Shirota relieves stress-associated symptoms by modulating the gut-brain interaction in human and animal models. Neurogastroenterol Motil. Jul 2016;28(7):1027-1036.
41. Kato-Kataoka A et al. Fermented milk containing Lactobacillus casei strain Shirota prevents the onset of physical symptoms in medical students under academic examination stress. Benef Microbes. 2016;7(2):153-156.
42. Kato-Kataoka A et al. Fermented Milk Containing Lactobacillus casei Strain Shirota Preserves the Diversity of the Gut Microbiota and Relieves Abdominal Dysfunction in Healthy Medical Students Exposed to Academic Stress. Appl Environ Microbiol. Jun 15 2016;82(12):3649-3658.
43. Andersson H et al. Oral Administration of Lactobacillus plantarum 299v Reduces Cortisol Levels in Human Saliva during Examination Induced Stress: A Randomized, Double-Blind Controlled Trial. Int J Microbiol. 2016;2016:8469018.
44. Messaoudi M et al. Assessment of psychotropic-like properties of a probiotic formulation (Lactobacillus helveticus R0052 and Bifidobacterium longum R0175) in rats and human subjects. Br J Nutr. Mar 2011;105(5):755-764.
45. Allen AP et al. Bifidobacterium longum 1714 as a translational psychobiotic: modulation of stress, electrophysiology and neurocognition in healthy volunteers. Transl Psychiatry. Nov 1 2016;6(11):e939.
46. Schmidt K et al. Prebiotic intake reduces the waking cortisol response and alters emotional bias in healthy volunteers. Psychopharmacology (Berl). May 2015;232(10):1793-1801.
47.
268. Turkozu D, Sanlier N. L-theanine, unique amino acid of tea, and its metabolism, health effects, and safety. Crit Rev Food Sci Nutr. May 24 2017;57(8):1681-1687.
269. Unno K, Tanida N, Ishii N, et al. Anti-stress effect of theanine on students during pharmacy practice: positive correlation among salivary alpha-amylase activity, trait anxiety and subjective stress. Pharmacol Biochem Behav. Oct 2013;111:128-135.
270. White DJ, de Klerk S, Woods W, Gondalia S, Noonan C, Scholey AB. Anti-Stress, Behavioural and Magnetoencephalography Effects of an L-Theanine-Based Nutrient Drink: A Randomised, Double-Blind, Placebo-Controlled, Crossover Trial. Nutrients. Jan 19 2016;8(1).
参考来源:
美国梅奥诊所
www.mayoclinic.org
美国心脏病协会
https://www.heart.org/
美国国立公众健康网
www.medlineplus.gov
美国医疗在线网
www.webmd.com
加拿大卫生部
www.hc-sc.gc.ca
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

